Xeomin® საქართველოში: ბოტულინოტოქსინის რეგისტრაცია, სამართლებრივი სტატუსი და პაციენტის უსაფრთხოების საზოგადოებრივი ჯანდაცვის მნიშვნელობა
შესავალი — ანალიტიკური კომენტარი
ბოტულინოტოქსინი ტიპი A თანამედროვე მედიცინის ერთ-ერთი ყველაზე ფართოდ გამოყენებული ბიოლოგიური პრეპარატია, რომელიც გამოიყენება როგორც ნევროლოგიური, ასევე დერმატოლოგიური და ესთეტიკური ჩვენებების შემთხვევაში. მიუხედავად ფართო პოპულარობისა, აღნიშნული პრეპარატი მიეკუთვნება მაღალი რისკის ბიოლოგიურ მედიკამენტებს, რაც ნიშნავს, რომ მისი წარმოება, რეგისტრაცია, გავრცელება და კლინიკური გამოყენება მკაცრ სამართლებრივ და სამედიცინო კონტროლს საჭიროებს [1].
პაციენტის უსაფრთხოება ამ კონტექსტში წარმოადგენს საზოგადოებრივი ჯანდაცვის პრიორიტეტს, რადგან ბიოლოგიური მედიკამენტები, განსხვავებით ქიმიური სინთეზის პრეპარატებისგან, შეიცავს ცოცხალი ორგანიზმებიდან მიღებულ კომპონენტებს, რაც მათ უსაფრთხოებასა და ეფექტიანობას განსაკუთრებულ რეგულაციას საჭიროებს [2].
საქართველოში ბოტულინოტოქსინის სხვადასხვა პრეპარატის რეგისტრაცია და გამოყენება მიმდინარეობს სახელმწიფო კონტროლის პირობებში. ერთ-ერთი ასეთი პრეპარატია Xeomin®, რომელიც წარმოადგენს ბოტულინოტოქსინის ტიპი A-ის შემცველ ბიოლოგიურ მედიკამენტს და ფლობს ოფიციალურ რეგისტრაციას საქართველოს სამედიცინო პროდუქციის სახელმწიფო რეესტრში. აღნიშნული საკითხის განხილვა მნიშვნელოვანია როგორც კლინიკური უსაფრთხოების, ისე პაციენტთა უფლებების დაცვისა და სამედიცინო ხარისხის უზრუნველყოფის თვალსაზრისით, რაც წარმოადგენს ისეთი პროფესიული პლატფორმების პრიორიტეტსაც, როგორიცაა https://www.sheniekimi.ge.
პრობლემის აღწერა
ბოტულინოტოქსინის გამოყენება ბოლო ორი ათწლეულის განმავლობაში მნიშვნელოვნად გაიზარდა, განსაკუთრებით ესთეტიკური მედიცინის სფეროში. თუმცა, მისი გამოყენება დაკავშირებულია გარკვეულ კლინიკურ და სამართლებრივ რისკებთან, განსაკუთრებით მაშინ, როდესაც პროდუქტი არ არის რეგისტრირებული ან გამოიყენება არასათანადო პირობებში [1].
საქართველოში, ისევე როგორც სხვა ქვეყნებში, საზოგადოებრივი ჯანდაცვის სისტემის ერთ-ერთი გამოწვევაა იმის უზრუნველყოფა, რომ ბაზარზე არსებული ბიოლოგიური მედიკამენტები აკმაყოფილებდნენ უსაფრთხოების, ხარისხისა და ეფექტიანობის საერთაშორისო სტანდარტებს.
Xeomin® წარმოადგენს ბოტულინოტოქსინის ტიპი A-ის შემცველ მედიკამენტს, რომლის საერთაშორისო არაპატენტირებული დასახელებაა botulinum toxin type A, ხოლო მისი მწარმოებელია გერმანული კომპანია Merz Pharma GmbH & Co. KGaA [3].
პრეპარატი წარმოდგენილია ლიოფილიზირებული ფხვნილის სახით, რომელიც გამოიყენება საინექციო ხსნარის მოსამზადებლად და მიეკუთვნება ბიოლოგიურ მედიკამენტთა კატეგორიას. მისი მოქმედების მექანიზმი ეფუძნება ნერვ-კუნთოვანი გადაცემის დროებით ბლოკირებას, რაც იწვევს კუნთის მოდუნებას და გამოიყენება როგორც სამედიცინო, ასევე ესთეტიკური ჩვენებების შემთხვევაში [5].
სამეცნიერო და კლინიკური ანალიზი
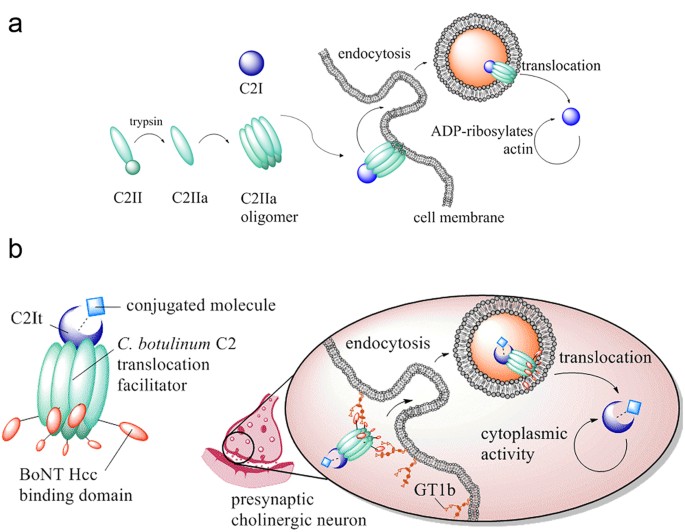
ბოტულინოტოქსინი წარმოადგენს ნეიროტოქსინს, რომელიც წარმოიქმნება ბაქტერიის Clostridium botulinum მიერ. იგი მოქმედებს ნერვულ დაბოლოებებზე, ბლოკავს აცეტილქოლინის გამოყოფას და იწვევს კუნთის დროებით პარალიზებას [5].
Xeomin®-ის ერთ-ერთი მნიშვნელოვანი ფარმაკოლოგიური თავისებურებაა ის, რომ იგი არ შეიცავს დამატებით კომპლექსურ ცილებს. ეს ფაქტორი მნიშვნელოვან გავლენას ახდენს მისი უსაფრთხოების პროფილზე, რადგან კომპლექსური ცილების არარსებობა ამცირებს იმუნური სისტემის რეაქციის განვითარების რისკს და ანტისხეულების წარმოქმნის ალბათობას [8].
იმუნოგენურობა წარმოადგენს ერთ-ერთ მთავარ პრობლემას ბიოლოგიური მედიკამენტების გამოყენებისას. როდესაც ორგანიზმი იწყებს ანტისხეულების წარმოქმნას პრეპარატის წინააღმდეგ, მისი ეფექტიანობა შეიძლება შემცირდეს. კვლევები აჩვენებს, რომ კომპლექსური ცილების გარეშე არსებული ფორმულაციები, როგორიცაა Xeomin®, დაკავშირებულია იმუნოგენურობის უფრო დაბალ რისკთან [5].
კლინიკური გამოყენებისას მნიშვნელოვანია შემდეგი ფაქტორები:
- დოზირების ინდივიდუალური განსაზღვრა
- ინექციის ტექნიკის სიზუსტე
- შენახვის პირობების დაცვა (2–8°C)
- პაციენტის მდგომარეობის მონიტორინგი
აღნიშნული ფაქტორების უგულებელყოფამ შეიძლება გაზარდოს არასასურველი ეფექტების განვითარების რისკი, მათ შორის კუნთის ზედმეტი სისუსტე ან დროებითი ფუნქციური დარღვევები [2].
სტატისტიკა და მტკიცებულებები
ბოტულინოტოქსინის გამოყენება მსოფლიოში მუდმივად იზრდება. საერთაშორისო მონაცემების მიხედვით, ბოტულინოტოქსინის ინექციები წარმოადგენს ერთ-ერთ ყველაზე ხშირად ჩატარებულ არაქირურგიულ პროცედურას [5].
საერთაშორისო კვლევების მიხედვით:
- ბოტულინოტოქსინის უსაფრთხოების პროფილი მაღალია, როდესაც იგი გამოიყენება რეგისტრირებული ფორმით და კვალიფიციური სპეციალისტის მიერ [2]
- სერიოზული გართულებების სიხშირე ძალიან დაბალია და უმეტეს შემთხვევაში დაკავშირებულია არასათანადო გამოყენებასთან
- იმუნოგენური რეაქციების სიხშირე ნაკლებია თანამედროვე ფორმულაციების შემთხვევაში, როგორიცაა Xeomin® [8]
ჯანმრთელობის მსოფლიო ორგანიზაცია ხაზს უსვამს, რომ ბიოლოგიური მედიკამენტების უსაფრთხო გამოყენების მთავარი წინაპირობა არის რეგისტრაცია, ხარისხის კონტროლი და ფარმაკოვიგილანსის სისტემა [1].
საერთაშორისო გამოცდილება
Xeomin® დამტკიცებულია მსოფლიოს წამყვანი მარეგულირებელი ორგანოების მიერ, რაც მიუთითებს მის უსაფრთხოებასა და ეფექტიანობაზე.
აშშ-ის სურსათისა და მედიკამენტების ადმინისტრაცია (FDA) ოფიციალურად ამტკიცებს ბოტულინოტოქსინის პრეპარატებს მხოლოდ მაშინ, როდესაც ისინი აკმაყოფილებენ უსაფრთხოების მკაცრ მოთხოვნებს [7].
ევროპის მედიკამენტების სააგენტო (EMA) ასევე ახორციელებს მკაცრ შეფასებას ბიოლოგიური მედიკამენტების რეგისტრაციამდე, რაც მოიცავს ხარისხის, ეფექტიანობისა და უსაფრთხოების მრავალდონიან შეფასებას [8].
გაერთიანებული სამეფოს მარეგულირებელი ორგანო MHRA დამატებით ახორციელებს ფარმაკოვიგილანსის სისტემის მონიტორინგს, რათა დროულად გამოვლინდეს შესაძლო არასასურველი მოვლენები [9].
ეს საერთაშორისო გამოცდილება მიუთითებს, რომ რეგისტრირებული ბიოლოგიური მედიკამენტები უსაფრთხოა, როდესაც გამოიყენება შესაბამისი სამედიცინო სტანდარტების დაცვით.
საქართველოს კონტექსტი
საქართველოს სამედიცინო პროდუქციის სახელმწიფო რეესტრის მონაცემებით, Xeomin® ფლობს მოქმედ რეგისტრაციას საქართველოში, რაც ნიშნავს, რომ მისი გამოყენება დაშვებულია მოქმედი კანონმდებლობის ფარგლებში [3].
რეგისტრაციის მონაცემები:
- Xeomin® 50 ერთეული
რეგისტრაციის ნომერი: № N-044603
რეგისტრაციის ვადა: 15.01.2026 – 15.01.2031 - Xeomin® 100 ერთეული
რეგისტრაციის ნომერი: № N-044604
რეგისტრაციის ვადა: 15.01.2026 – 15.01.2031
პრეპარატი გაიცემა მხოლოდ რეცეპტით, რაც წარმოადგენს პაციენტის უსაფრთხოების დაცვის მნიშვნელოვან მექანიზმს.
საქართველოს საზოგადოებრივი ჯანდაცვის სისტემა, რომლის შესახებ ინფორმაცია ხელმისაწვდომია https://www.publichealth.ge, უზრუნველყოფს ბიოლოგიური მედიკამენტების რეგულაციას და უსაფრთხოების მონიტორინგს.
ასევე მნიშვნელოვანია აკადემიური და პროფესიული სტანდარტების განვითარება, რაც მხარდაჭერილია ისეთი პლატფორმების მიერ, როგორიცაა https://www.gmj.ge, სადაც განიხილება მედიკამენტების უსაფრთხოებისა და ხარისხის საკითხები.
პროდუქტის ხარისხის კონტროლისა და სერტიფიკაციის საკითხები ასევე მნიშვნელოვანია, რაც დაკავშირებულია საერთაშორისო სტანდარტებთან და შესაბამისი ინფორმაციის მიღება შესაძლებელია https://www.certificate.ge-ზე.
მითები და რეალობა
მითი: ყველა ბოტულინოტოქსინი ერთნაირია
რეალობა: ბოტულინოტოქსინის სხვადასხვა პრეპარატი განსხვავდება წარმოების ტექნოლოგიით, ფორმულაციით და უსაფრთხოების პროფილით [5].
მითი: ბოტულინოტოქსინი ყოველთვის საშიშია
რეალობა: რეგისტრირებული და სწორად გამოყენებული პრეპარატი უსაფრთხოა და ფართოდ გამოიყენება მედიცინაში [1].
მითი: ბოტულინოტოქსინი მხოლოდ ესთეტიკური მიზნით გამოიყენება
რეალობა: იგი გამოიყენება მრავალი სამედიცინო მდგომარეობის სამკურნალოდ, მათ შორის ნევროლოგიური დაავადებების შემთხვევაში [2].
ხშირად დასმული კითხვები (Q&A)
არის თუ არა Xeomin® ლეგალურად დაშვებული საქართველოში?
დიახ, Xeomin® ფლობს მოქმედ რეგისტრაციას და მისი გამოყენება დაშვებულია კანონმდებლობის ფარგლებში [3].
შეიძლება თუ არა მისი შეძენა რეცეპტის გარეშე?
არა, იგი გაიცემა მხოლოდ ექიმის რეცეპტით.
არის თუ არა იგი უსაფრთხო?
დიახ, როდესაც გამოიყენება რეგისტრირებული ფორმით და კვალიფიციური ექიმის მიერ [2].
არის თუ არა Xeomin® იგივე, რაც Botox®?
არა, ისინი განსხვავებული ბიოლოგიური პრეპარატებია, მიუხედავად იმისა, რომ მიეკუთვნებიან ერთსა და იმავე ჯგუფს [5].
დასკვნა — საზოგადოებრივი ჯანდაცვის პერსპექტივით
Xeomin® წარმოადგენს ბოტულინოტოქსინის ტიპი A-ის შემცველ ბიოლოგიურ მედიკამენტს, რომელიც ფლობს მოქმედ რეგისტრაციას საქართველოში და აკმაყოფილებს საერთაშორისო რეგულატორულ სტანდარტებს.
პაციენტის უსაფრთხოება დამოკიდებულია არა მხოლოდ პრეპარატის ხარისხზე, არამედ მისი გამოყენების პირობებზე. რეგისტრირებული მედიკამენტების გამოყენება, კვალიფიციური ექიმის ჩართულობა და სახელმწიფო კონტროლის არსებობა წარმოადგენს საზოგადოებრივი ჯანდაცვის უსაფრთხოების მთავარ საფუძველს.
საქართველოში მოქმედი რეგულატორული სისტემა უზრუნველყოფს ბიოლოგიური მედიკამენტების უსაფრთხო გამოყენებას, თუმცა მნიშვნელოვანია საზოგადოებრივი ცნობიერების ამაღლება, რათა პაციენტებმა მიიღონ ინფორმირებული გადაწყვეტილებები და გამოიყენონ მხოლოდ ოფიციალურად რეგისტრირებული პრეპარატები.
წყაროები
- World Health Organization. Guidelines on the quality, safety and efficacy of biotherapeutic protein products. Available at: https://www.who.int/publications
- European Medicines Agency. Botulinum toxin products safety overview. Available at: https://www.ema.europa.eu
- საქართველოს სამედიცინო პროდუქციის სახელმწიფო რეესტრი (mis.ge). Xeomin® რეგისტრაციის მონაცემები. Available at: https://mis.ge
- Merz Pharma GmbH & Co. KGaA. Xeomin® Summary of Product Characteristics. Available at: https://merz.com
- Carruthers J, Carruthers A. Botulinum toxin type A pharmacology and clinical use. Dermatologic Surgery. Available at: https://journals.lww.com
- Public Health Institute of Georgia. Injectable medicines regulation and patient safety framework. Available at: https://www.publichealth.ge
- Food and Drug Administration. Approved botulinum toxin products database. Available at: https://www.fda.gov
- European Medicines Agency. Regulatory status of botulinum toxin type A products. Available at: https://www.ema.europa.eu
- Medicines and Healthcare products Regulatory Agency. Botulinum toxin regulatory overview. Available at: https://www.gov.uk/mhra