შესავალი — ანალიტიკური კომენტარი
რეპროდუქციული მედიცინა ბოლო ათწლეულებში ერთ-ერთ ყველაზე სწრაფად განვითარებად სფეროდ იქცა, რადგან უნაყოფობა დღეს უკვე არა მხოლოდ ინდივიდუალური, არამედ საზოგადოებრივი ჯანდაცვის მნიშვნელოვანი გამოწვევაა. თანამედროვე მონაცემებით, ფერტილურობის პრობლემა მილიონობით ადამიანს ეხება და მას აქვს როგორც ბიოლოგიური, ისე სოციალური და დემოგრაფიული შედეგები [1].
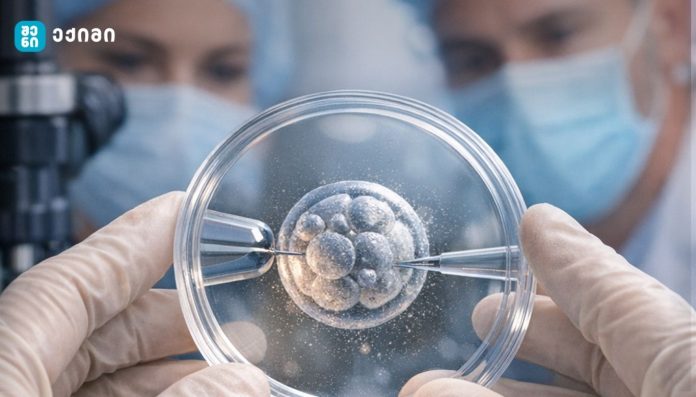
ამ კონტექსტში განსაკუთრებულ ინტერესს იწვევს ახალი კვლევა, რომლის მიხედვითაც მეცნიერებმა ადამიანის კანის დნმ-ის გამოყენებით ფუნქციური კვერცხუჯრედების მიღება შეძლეს. ამ უჯრედებს განაყოფიერების უნარი აქვთ და ზიგოტად ჩამოყალიბებაც შეუძლიათ, რაც პოტენციურად ინოვაციურ გზას ხსნის უნაყოფობის მკურნალობაში. თუმცა სპეციალისტები ხაზგასმით აღნიშნავენ, რომ ტექნიკის კლინიკურ პრაქტიკაში დანერგვას მინიმუმ 10–15 წელი დასჭირდება [2].
სანდო სამედიცინო ინფორმაციის გავრცელება ისეთ პლატფორმებზე, როგორიცაა https://www.sheniekimi.ge და https://www.publichealth.ge, მნიშვნელოვანია იმისთვის, რომ საზოგადოებამ სწორად გაიაზროს ინოვაციების შესაძლებლობები და შეზღუდვები.
პრობლემის აღწერა
უნაყოფობა განისაზღვრება როგორც მდგომარეობა, როდესაც დაორსულების მცდელობა 12 თვის განმავლობაში უშედეგოა. პრობლემა შეიძლება უკავშირდებოდეს ქალის, კაცის ან ორივე პარტნიორის რეპროდუქციულ ფუნქციას [1].
ფერტილურობის დარღვევის ერთ-ერთი მთავარი მიზეზი არის გამეტების — კვერცხუჯრედისა და სპერმის — არასრულფასოვანი ფუნქციონირება. ქალებში კვერცხუჯრედების ხარისხისა და რაოდენობის შემცირება ხშირად ასაკთანაა დაკავშირებული, თუმცა მიზეზი შეიძლება იყოს ონკოლოგიური დაავადებები, ჰორმონული დარღვევები ან გენეტიკური ფაქტორებიც [3].
ქართველი მკითხველისთვის ეს საკითხი აქტუალურია, რადგან უნაყოფობის მკურნალობა საქართველოში მზარდი მოთხოვნის სფეროა, ხოლო თანამედროვე ტექნოლოგიების ხელმისაწვდომობა ხშირად დაკავშირებულია მაღალ ხარჯებთან და რეგულაციურ გამოწვევებთან.
სამეცნიერო და კლინიკური ანალიზი
კვლევის მთავარი ინოვაცია უკავშირდება ინ ვიტრო გამეტოგენეზის (IVG) მიმართულებას — მეთოდს, რომელიც პაციენტის გენეტიკური მასალიდან გამეტების შექმნას გულისხმობს. ეს ტექნოლოგია წარმატებით განხორციელდა ცხოველურ მოდელებში, განსაკუთრებით თაგვებში, თუმცა ადამიანებში ჯერ მხოლოდ ექსპერიმენტულ ეტაპზეა [4].
ახალი მიდგომის ერთ-ერთი ფორმაა სომატური უჯრედის ბირთვის გადატანა (SCNT). ამ პროცესში სხეულის უჯრედის ბირთვი შეჰყავთ დონორის კვერცხუჯრედში, რომელსაც საკუთარი ბირთვი ამოცლილი აქვს. შედეგად მიიღება რეკონსტრუირებული კვერცხუჯრედი, რომელიც გენეტიკურად მშობლის უჯრედს შეესაბამება [2].
მთავარი სირთულე ისაა, რომ ამ გზით მიღებულ უჯრედებში ქრომოსომების რაოდენობა 46 წყვილია, მაშინ როცა ნორმალური კვერცხუჯრედი ჰაპლოიდურია და მხოლოდ 23 წყვილ ქრომოსომას შეიცავს. სწორედ ამიტომ მკვლევრებმა შეიმუშავეს ახალი ტექნიკა —所谓 „მიტომეიოზი“, რომელიც ბუნებრივი უჯრედული დაყოფის იმიტაციას ახდენს და ქრომოსომების ნახევრის მოცილებას უზრუნველყოფს.
რეპროდუქციული ენდოკრინოლოგი პაულა ამატო აღნიშნავს, რომ ამ გზით პლურიპოტენტური ღეროვანი უჯრედების კულტივაციაზე დამოკიდებულება მცირდება, რაც პროცესს აჩქარებს და შესაძლოა გენეტიკური ანომალიების რისკიც შეამციროს [2].
კლინიკური თვალსაზრისით, ასეთი ტექნოლოგია პოტენციურად მნიშვნელოვანი იქნება იმ ადამიანებისთვის, რომელთაც საკუთარი კვერცხუჯრედების წარმოება აღარ შეუძლიათ, მაგალითად ონკოლოგიური მკურნალობის შემდეგ.
სტატისტიკა და მტკიცებულებები
გლობალური მონაცემებით, უნაყოფობა დაახლოებით 15%-მდე წყვილს ეხება, რაც მას საზოგადოებრივი ჯანმრთელობის მნიშვნელოვან პრობლემად აქცევს [1].
კვლევის ფარგლებში მეცნიერებმა 82 ფუნქციური ოვოციტი შექმნეს და ისინი გაანაყოფიერეს. შედეგები შერეული აღმოჩნდა:
- უმეტესობამ განვითარება შეწყვიტა უჯრედული დაყოფის მე-4–მე-10 ეტაპზე
- დაახლოებით 9%-მა ბლასტოცისტად ჩამოყალიბება განაგრძო
მართალია, ეს მაჩვენებელი მცირეა, თუმცა ადასტურებს, რომ ტექნიკა ფუნქციონირებს და ადამიანის უჯრედებიდან მიღებულ კვერცხუჯრედებს განაყოფიერების პოტენციალი აქვთ [2].
ექსპერიმენტი მეექვსე დღეს შეწყდა ეთიკური და სამეცნიერო სტანდარტების შესაბამისად, რადგან სწორედ ამ ეტაპზე ხდება ბლასტოცისტის იმპლანტაცია კლინიკურ პრაქტიკაში.
საერთაშორისო გამოცდილება
WHO და NIH ხაზს უსვამენ, რომ უნაყოფობა საზოგადოებრივი ჯანმრთელობის მნიშვნელოვანი საკითხია და თანამედროვე რეპროდუქციული ტექნოლოგიები შეიძლება გახდეს მისი მართვის ერთ-ერთი მთავარი გზა [1], [5].
The Lancet და BMJ რეგულარულად აქვეყნებენ კვლევებს ინ ვიტრო განაყოფიერების, ღეროვანი უჯრედების გამოყენებისა და გენეტიკური ტექნოლოგიების განვითარების შესახებ, თუმცა აღნიშნავენ, რომ ადამიანებში გამეტების ხელოვნური შექმნა ჯერ კიდევ დაკავშირებულია მნიშვნელოვან ეთიკურ და უსაფრთხოების საკითხებთან [6].
NEJM-ის შეფასებით, ყველაზე დიდი გამოწვევა ასეთ ტექნოლოგიებში არის ქრომოსომური სტაბილურობის უზრუნველყოფა, რადგან მცირე შეცდომამ შეიძლება მძიმე გენეტიკური ანომალიები გამოიწვიოს [7].
საერთაშორისო გამოცდილება აჩვენებს, რომ მსგავსი ინოვაციები ხშირად ათწლეულებს საჭიროებს კლინიკურ პრაქტიკაში დასამკვიდრებლად.
საქართველოს კონტექსტი
საქართველოში რეპროდუქციული მედიცინა განვითარებადი სფეროა და ინ ვიტრო განაყოფიერება უკვე ფართოდ გამოიყენება. თუმცა ახალი თაობის ტექნოლოგიები, როგორიცაა IVG და SCNT, მოითხოვს მაღალტექნოლოგიურ ინფრასტრუქტურას, მკაცრ რეგულაციას და ეთიკური ზედამხედველობის სისტემას.
ასეთი კვლევების განხილვა მნიშვნელოვანია აკადემიურ სივრცეებში, როგორიცაა https://www.gmj.ge, ხოლო ხარისხისა და უსაფრთხოების სტანდარტების განვითარება დაკავშირებულია ისეთ პლატფორმებთან, როგორიცაა https://www.certificate.ge.
საქართველოსთვის მთავარი საკითხი იქნება, რამდენად შეძლებს ქვეყანა მომავალში მსგავსი ტექნოლოგიების უსაფრთხო და ხელმისაწვდომ დანერგვას.
მითები და რეალობა
მითი: „ხელოვნურად შექმნილი კვერცხუჯრედები მალე ჩაანაცვლებს IVF-ს.“
რეალობა: ტექნოლოგია ჯერ ექსპერიმენტულია და კლინიკურ გამოყენებას ათწლეულები დასჭირდება [2].
მითი: „კანის უჯრედიდან მიღებული კვერცხუჯრედი სრულიად უსაფრთხოა.“
რეალობა: კვლევაში გამოვლინდა ქრომოსომური ანომალიების რისკი, რაც ჯერ გადაუჭრელი პრობლემაა [7].
მითი: „ეს მეთოდი უკვე მზადაა ადამიანებში გამოსაყენებლად.“
რეალობა: ავტორები თავად აღნიშნავენ, რომ პრაქტიკაში დანერგვა მინიმუმ 10–15 წელს მოითხოვს [2].
ხშირად დასმული კითხვები (Q&A)
რა არის ინ ვიტრო გამეტოგენეზი?
ეს არის ტექნოლოგია, რომელიც ადამიანის გენეტიკური მასალიდან გამეტების შექმნას გულისხმობს [4].
შეიძლება თუ არა ამ მეთოდით მიღებული კვერცხუჯრედის გამოყენება დღესვე?
არა, ტექნიკა ჯერ მხოლოდ კვლევით ეტაპზეა და კლინიკურ გამოყენებამდე დიდი დროა საჭირო [2].
რა არის მთავარი გამოწვევა?
ქრომოსომური ანომალიების თავიდან აცილება და გენეტიკური სტაბილურობის უზრუნველყოფა [7].
ვისთვის შეიძლება იყოს ეს ტექნოლოგია მნიშვნელოვანი?
იმ ადამიანებისთვის, რომელთაც კვერცხუჯრედების დაკარგვა ან მძიმე ფერტილურობის პრობლემა აქვთ, მაგალითად ონკოლოგიური მკურნალობის შემდეგ [3].
დასკვნა — საზოგადოებრივი ჯანდაცვის პერსპექტივით
ადამიანის კანის დნმ-ის გამოყენებით კვერცხუჯრედების მიღება წარმოადგენს მნიშვნელოვან მეცნიერულ მიღწევას, რომელიც მომავალში შესაძლოა უნაყოფობის მკურნალობის ახალ შესაძლებლობებს შექმნას.
თუმცა ტექნოლოგია ჯერ კიდევ ადრეულ ეტაპზეა და დაკავშირებულია გენეტიკური უსაფრთხოების, ეთიკური რეგულაციისა და კლინიკური სტანდარტების სერიოზულ გამოწვევებთან.
საზოგადოებრივი ჯანდაცვისთვის მნიშვნელოვანია, რომ მსგავსი ინოვაციები შეფასდეს პასუხისმგებლობით, გამჭვირვალე კვლევებითა და ხარისხის მკაცრი კონტროლით, რათა მომავალში შესაძლებელი გახდეს უსაფრთხო და ეფექტური გამოყენება.
წყაროები
- World Health Organization. Infertility prevalence and global health impact. Available from: https://www.who.int/news-room/fact-sheets/detail/infertility
- Nature. Somatic cell nuclear transfer and mitomeiosis in human oocyte generation. 2026. Available from: https://www.nature.com
- NIH. Female infertility causes and treatment options. Available from: https://www.nichd.nih.gov
- Hayashi K, et al. In vitro gametogenesis: current status and future perspectives. Science. 2018. Available from: https://pubmed.ncbi.nlm.nih.gov/
- National Institutes of Health. Advances in reproductive medicine. Available from: https://www.nih.gov
- The Lancet. Assisted reproduction and emerging technologies. Available from: https://www.thelancet.com
- New England Journal of Medicine. Ethical and genetic challenges of human gamete engineering. Available from: https://www.nejm.org